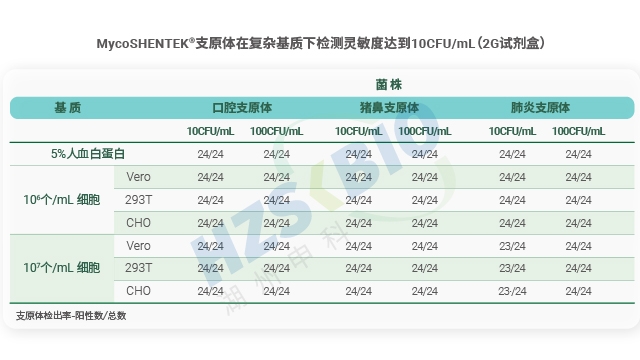
支原体检测 NAT 方法验证需满足全球药典对检测限、专属性、耐用性、可比性等关键指标的要求,且 EP、USP 新草案提出更严格标准。检测限(LOD)方面,EP 要求针对每种支原体确定临界值,需 3 次单独 10 倍梯度稀释、共 24 个检测数据,95% 检出浓度达标;USP 要求标准菌株浓度≤10 CFU/mL 或 100 GC/mL,≥24 次检测数据支持统计分析;ChP 未明确支原体专属要求,但需满足 “微生物检出下限数量” 设定标准。专属性上,EP 建议测试革兰氏阳性菌交叉污染,USP 要求生信分析与实际样品验证结合,ChP 强调外来成分不干扰试验。耐用性方面,EP 需验证试剂浓度、提取与反应程序变化,USP 涵盖设备、反应体系等参数波动。可比性上,EP 要求 NAT 法与药典法 LOD 及特异性对比,替代培养法需达 10 CFU/mL,替代指示细胞法需达 100 CFU/mL,USP 则视样品基质情况要求可比性研究。
EP 新规明确支原体验证菌株 GC/CFU 比值<10,需在指数阶段收获以保障活性与分散性。北京重组药物支原体检测可比性验证
支原体 NAT 检测的准确性与可靠性受多重因素综合影响,需从人员、方法、设备、试剂耗材、实验室环境五方面严格把控。人员需接受专业培训,熟练掌握 PCR 技术理论与实操流程,积累足够经验并具备责任心,确保操作规范性。方法建立需遵循合理流程并完成充分验证,避免因方法缺陷导致结果偏差。设备方面,PCR 仪与前处理设备的性能、精度、稳定性及定期校准至关重要,直接影响检测数据的重复性。试剂耗材需满足要求:前处理试剂能应对复杂样本基质、耐受常见干扰,检测试剂经性能验证且批间稳定性良好,同时需选用质量合格的耗材。实验室需合理布局,建立完善的管理规范与污染防控措施,为检测提供洁净、可控的环境,避免外部因素干扰。
天津重组药物支原体检测培养法支原体检测取样需按产品体积设计,10-1000mL 样品取总体积 1%,保障结果代表性。
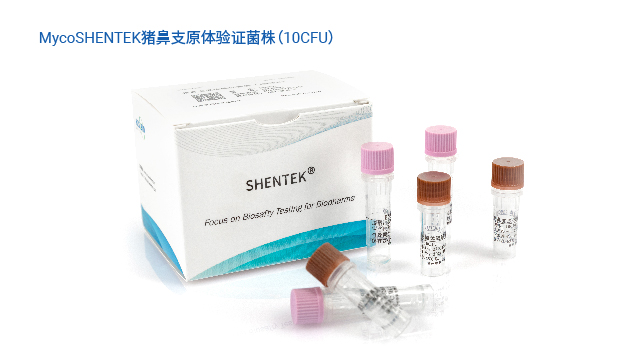
湖州申科的支原体验证菌株是支原体检测 NAT 方法验证的可靠选择,具备多重质量保障。菌株来源可靠,均取自国内外认可的合规机构验证菌株标准盘,溯源至美国模式菌种收集中心(ATCC)、中国兽医微生物菌种保藏管理中心(CVCC)等正规保藏机构,获得正式授权商用,如口腔支原体、肺炎支原体溯源至 ATCC,猪鼻支原体溯源至 CVCC。菌株生产在 BSL-2 生物安全实验室开展,符合国家生物安全法标准,针对不同菌株特性逐个优化生产工艺,涵盖超 10 种菌株的主代与工作代。质控环节严谨,采用固体平皿培养法测定 CFU(菌落形成单位),冻存前后均进行检测,确保菌落易观察分离与计数准确性;同时联合官方机构建立数字 PCR 标定方法,开展实验室间对比验证,监控 GC/CFU 比值,保障菌株活性与定量准确性,标定浓度涵盖 10CFU 和 100CFU,满足 NAT 方法验证需求。
湖州申科推出的 MycoSHENTEK® 支原体验证菌株,符合全球药典要求,目前已提供口腔支原体、肺炎支原体、猪鼻支原体三种菌株,后续将逐步扩充其他验证用菌株。该系列菌株溯源至全球保藏机构并获得正式授权,经培养法测定 CFU(菌落形成单位)与 dPCR 法测定 GC(基因组拷贝数),实现准确定量标定,浓度涵盖 10CFU 和 100CFU 两种规格,每盒含 3 管,完全满足支原体检测方法验证需求。菌株经灭活处理,无风险,使用时只需加入相应体积样品基质即可开展验证,操作便捷,同时通过双重定量检测确保质量可控,为 NAT 方法验证提供可靠的标准物质支撑。
支原体检测中高浓度 DMSO 会抑制 PCR 反应,湖州申科通过优化样品预处理流程,有效消除该干扰。
抑制物质检测是支原体培养法的关键前置环节,旨在排除供试品中抑制成分对检测的干扰。湖州申科按 USP 标准执行:对供试品进行一次抑制物质检测,若生产方法发生变化可能影响支原体检测结果,需重复该检测。检测通过两组平行实验对比实现:一组培养基加入供试品,另一组不加供试品,同步开展营养特性测试,判断供试品是否含抑制物质。若检出抑制物质,需通过适当方法中和或抵消其作用,例如使用不含抑制剂的底物,或将供试品稀释在更大体积的培养基中,确保支原体能在检测体系中正常生长,避免因抑制成分导致检测结果失真。
支原体检测 NAT 法验证需包含空白限测试,确保无基质背景干扰。湖北重组药物支原体检测技术服务
湖州申科支原体检测快速版试剂盒 2-2.5 小时出结果,适配紧急放行,满足细胞疗法时效需求。北京重组药物支原体检测可比性验证
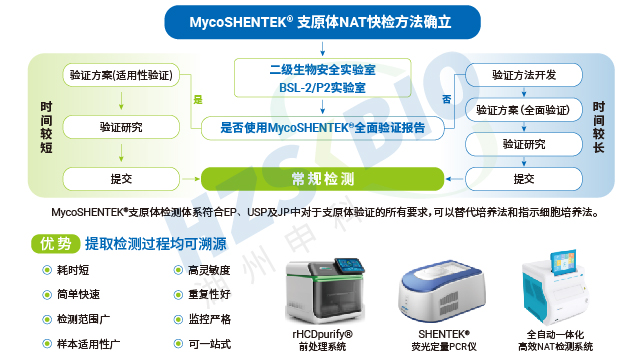
湖州申科构建了具有完备资质的支原体技术服务平台,为企业提供多元化支持。平台拥有 BSL-2/P2 微生物实验室备案资质,遵循 GMP-like 质量体系,具备支原体培养法、指示细胞法与 qPCR 法的检测及验证能力,配备符合药典要求的支原体标准菌株库与高灵敏度培养基(含液体、固体、半流体)。企业已通过 ISO13485:2016 质量管理体系认证(证书号 MD 709873),检测中心获得 CNAS 认证(注册号 CNAS L21942),符合 ISO/IEC 17025:2017 标准,具备国际互认资质。平台可提供多元化技术服务,包括支原体 qPCR 法检测能力建立、实验员能力考核、质量体系与流程搭建、实验室设计方案优化,以及样品检测(三种方法)、样品适用性验证、方法学验证、传统法与 qPCR 法比对、特殊菌株定制生产等,申报阶段可配合客户与监管机构完成现场审计。
北京重组药物支原体检测可比性验证