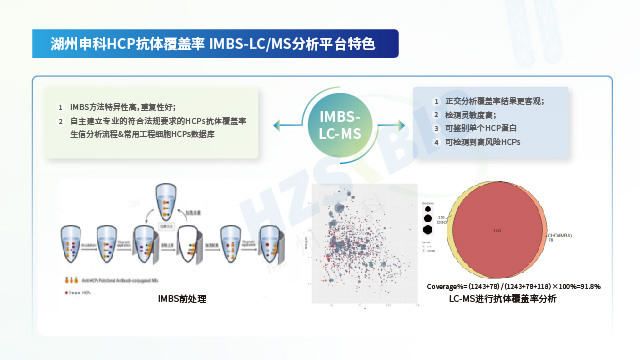
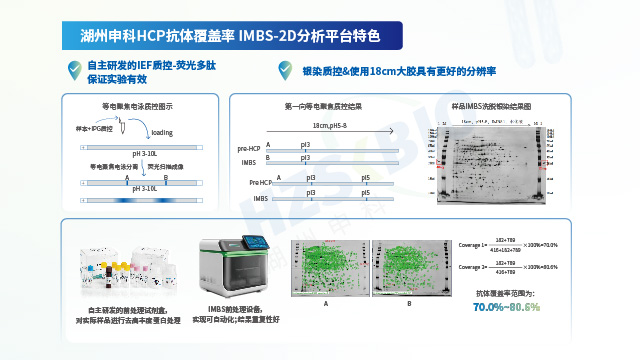
湖州申科生物凭借自主可控的供应链与经严格验证的技术性能,确保 HCP 检测试剂盒的长期稳定供应及出色分析能力。一方面,公司实现关键物料自研自产:校准品通过冻干工艺大规模生产,能稳定储存 10 年以上;抗体经大动物免疫制备,产量可支撑≥10,000 盒试剂盒生产,确保同批次抗体连续供应超 10 年;试剂盒经多批次验证,批内与批间一致性表现良好。另一方面,所有产品均参照 ICH Q2(R2)及 ICH M10 法规要求完成验证:以大肠杆菌(E.coli)HCP 产品为例,其线性范围(1-243 ng/mL)的 R²>0.999,各浓度点回收率偏差≤5%;准确度处于 81.2%-111.6% 区间,中间精密度 CV 值为 5.7%-12.4%;定量限(LLOQ)低至 1.5 ng/mL,且对 CHO、HEK293 等多种宿主细胞的交叉反应均低于检测限。同时,借助二维电泳(检出 826 个蛋白点)与质谱法(鉴定 2204 个蛋白点)对校准品进行双重表征,并运用 IMBS-2D(覆盖率 > 70%)与 IMBS-MS(覆盖率 84.7%)正交技术验证抗体覆盖率,从源头保障检测结果的全面性与可靠性。
不同技术平台获得的抗体覆盖率水平不一样,一般覆盖率水平从高到低依次IMBS-MS>IMBS-2D>2D-Western Blot。毕赤酵母宿主细胞蛋白(HCP)残留检测方法对比
法规推荐的抗体覆盖率评估方法主要分为两类:一类是传统 2D-WB 法,另一类是基于抗体亲和的免疫捕获类方法。传统 2D-WB 法存在诸多不足,如需对蛋白进行变性处理、样品需前处理(会破坏蛋白天然表位)、转膜效率较低、易出现非特异性反应等,因此难以准确反映真实的覆盖率水平。湖州申科自主研发了免疫磁珠捕获分离技术(immunomagnetic beads separation,IMBS),该技术借助免疫磁珠的半液态特性,能在悬浮状态下与 HCP 样本充分混匀并结合;整个过程中蛋白无需变性,且结合方式与 ELISA 检测条件相近,从而可获得更贴近真实情况的覆盖率结果。
毕赤酵母宿主细胞蛋白(HCP)残留检测方法对比抗体覆盖率评估属于定性分析,要求是稳定性好,灵敏度高,与ELISA检测的原理相似,确保结果准确可靠。
MDCK(Madin-DarbyCanineKidney,马丁达比犬肾上皮细胞)细胞系是源于犬肾的持续性细胞系,广泛应用于流感病毒增殖纯化、流感疫苗生产等过程,作为细胞基质使用。凭借高病毒产量与滴度、无适应性突变、易驯化等优势,MDCK细胞已成为业界公认的流感病毒毒株分离及流感疫苗生产适配细胞系。和其他产品杂质类似,MDCK宿主残留蛋白(HCP)可能对生物制品的安全性与有效性产生不良影响,因此在生产监测、产品放行等环节,需对其开展定量研究并实施严格控制。SHENTEK®MDCK HCP残留检测试剂盒(一步酶联免疫吸附法),是湖州申科生物自主研发、拥有完全自主知识产权且关键试剂实现全国产化的MDCK HCP通用检测试剂盒。该试剂盒适用于基于MDCK细胞基质的病毒增殖纯化、疫苗生产等过程,可对其中的MDCK宿主残留蛋白进行定量检测,且操作步骤简便快捷、检测专一性高、性能稳定可靠。
大肠埃希氏菌(Escherichiacoli,简称E.coli,又称大肠杆菌)作为模式微生物,在生命科学研究领域应用较多。伴随基因治疗产业的快速发展,它还成为质粒DNA(pDNA)生产的主要宿主菌。质粒样品常规提取工艺中,常使用强碱性溶液进行细胞裂解与蛋白质变性,这种处理使其中的宿主细胞蛋白(HCPs)与传统物理破碎法得到的HCPs差异明显,进而导致采用免疫学原理的检测方法时,残留检测结果偏差较大。湖州申科生物的E.coli克隆菌碱裂HCP残留检测试剂盒,适用于大肠埃希氏菌(即大肠杆菌)克隆菌株的HCPs检测,涵盖DH5α、Top10、JM109等常见菌株。该试剂盒的抗体制备过程中,采用碱裂工艺制备的HCPs免疫动物,得到专属抗体,可用于经碱液裂解工艺处理后的宿主细胞蛋白(HCPs)定量检测。
湖州申科系列HCP检测产品均进行了校准品的表征分析,抗体覆盖率分析。
美国药典 USP 通则 <1132.1>《质谱法测定生物药中残留宿主细胞蛋白》(Residual Host Cell Protein Measurement in Biopharmaceuticals by Mass Spectrometry),主要内容是介绍 LC-MS 技术在宿主细胞残留蛋白检测中的应用。该通则围绕样品制备、质谱测试条件建立、数据分析、质谱方法验证等维度,详细说明质谱技术应用于 HCPs 检测的优势及需注意的事项。作为先进的分析技术平台,质谱技术在 HCPs 分析中的应用,无论是单独使用,还是与 ELISA 及其他分析方法联合使用,都能帮助生产企业在产品全生命周期中更清晰地理解并建立 HCPs 检测方法,进而保障产品质量稳定。
遵循严格且科学的宿主细胞蛋白残留检测标准,是确保产品顺利达标的重要基础条件。
上海ELISA法宿主细胞蛋白(HCP)残留检测抗体制备总蛋白检测差异是 HCP 免疫检测结果不同的原因之一。毕赤酵母宿主细胞蛋白(HCP)残留检测方法对比
美国药典(USP)1132 章节中,推荐的 HCP 抗体纯化方式有两种,分别是 Protein A/Protein G 亲和柱层析法与 HCP 抗原亲和柱层析法。这两种方法各有特点与不足,且均满足监管层面的要求。在实际应用场景中,针对不同产品,两种方法可能造成检测结果的差异。两种方法所获抗体的关键差异,在于 HCP 抗体有效含量的占比不同。其中,HCP 抗原亲和柱层析法的有效含量占比明显更高,但该方法存在部分 HCP 抗体流失的情况,这会使得针对特定样本的检测结果低于前者,因此企业在实际建立检测方法时,需开展充分评估。此外,HCP 抗原亲和柱层析法对纯化工艺的要求更为严格,若要确保抗体的批间一致性,需重点考察 HCP 抗原柱的制备工艺、柱子的使用寿命以及再次制备时的一致性等关键问题。
毕赤酵母宿主细胞蛋白(HCP)残留检测方法对比