医疗器械(如输液器、注射器、植入式设备)若携带内毒素,可能通过血液、组织接触引发异常反应或炎症反应。其检测需遵循 “模拟临床使用” 原则:采用浸提液(如 0.9% 氯化钠溶液或注射用水)在 37℃±1℃下浸提器械表面内毒素,再通过 LAL 或 rFC 法检测浸提液。不同器械的内毒素限值差异明显:一次性输液器需≤0.5 EU/device,植入式心脏瓣膜则要求更严格(≤0.06 EU/device)。检测时需注意器械材质对浸提效率的影响,如塑料类器械可能吸附内毒素,需优化浸提时间(通常≥1 小时)或采用超声辅助提取,确保残留内毒素被充分检出。
开展细菌内毒素检测的操作过程,需防止样品受到外源性污染。北京化学制药内毒素检测动态显色法鲎试剂
实验数据充分证明,内毒素检测重组级联试剂(rCR)与天然鲎试剂的检测结果具有高度等效性,可实现方法无缝切换。对细胞培养辅料、冻干甲型肝炎疫苗、单抗 A/B 等 8 类代表性样品的平行检测显示,rCR 的检测平均值为 0.001-0.026EU/mL,天然鲎试剂为 0.002-0.034EU/mL,两者偏差≤0.003EU/mL。加标回收率方面,rCR 为 70%-175.4%,天然鲎试剂为 82.2%-156.6%,均处于 50%-200% 的合格范围。批内精密度上,rCR 的 CV 值为 0.524%-14.716%,天然鲎试剂为 0.908%-12.348%,均满足法规对精密度的要求。这种等效性确保了实验室在切换至重组试剂时,历史数据和工艺控制标准的连续性,降低方法转换风险。
细菌内毒素检测动态显色法鲎试剂含蛋白酶的样本致假阳性时,可稀释后 70℃加热 5-15min 灭活,再做内毒素检测。
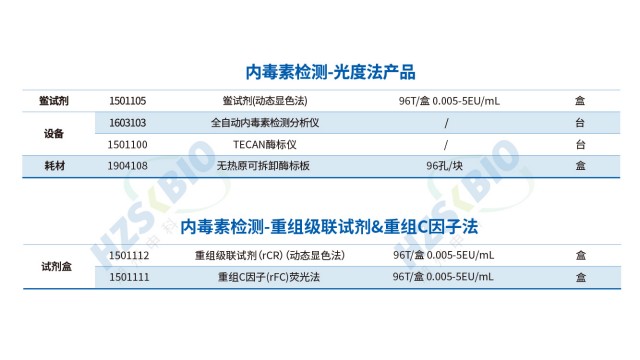
重组试剂(rCR、rFC)是解决 LER 的重要工具,优化内毒素检测性能。重组鲎试剂(rCR)通过基因工程表达 C、B 因子及凝固酶原,剔除 G 因子,完全模拟天然鲎级联反应,灵敏度达 0.005EU/mL,与天然方法桥接容易,能避免 LPS 结构变化导致的假阴性;重组 C 因子(rFC)灵敏度 0.005-5EU/mL,性状稳定、均一性好,虽需荧光酶标仪,但对部分 LER 场景(如无蛋白质干扰)适配性强。二者摆脱了天然鲎试剂的局限,为内毒素检测提供更抗 LER 的选择,契合行业技术趋势。
样品中的脂质体与表面活性剂,会通过不同机制干扰内毒素检测,需结合基质特性选择处理方式。脂质体的干扰体现在两方面:一是脂质双分子层会包裹内毒素,使其无法与鲎试剂接触,导致假阴性;二是脂质体的胶体性质会干扰凝胶形成(凝胶法)或光度信号读取(浊度 / 显色法)。针对完整脂质体制剂,可先用生理盐水稀释降低脂质体浓度,减少包裹作用;若需彻底释放内毒素,还可使用 DMSO、乙醇或甲醇等溶剂裂解脂质体,暴露被包裹的内毒素。表面活性剂的干扰则源于其对物质结构的改变:既可能破坏内毒素的聚集体结构,影响其活性;又可能导致鲎试剂中蛋白质变性,抑制反应。对此,可通过内毒素检查用水或生理盐水稀释样品,降低表面活性剂浓度,消除其对结构的破坏作用。这些针对性处理能有效解决脂质体与表面活性剂的干扰,确保内毒素检测结果真实可靠。
湖州申科内毒素检测服务含低内毒素回收,通过不同样品前处理方式搭配多种检测方法,较大程度解决LER问题。
内毒素检测方法易受样品基质干扰,法规要求在方法应用前必须进行干扰验证,选择标准曲线中点或一个靠近中点的内毒素浓度,作为供试品干扰试验种添加的内毒素浓度计算回收率,若回收率在 50%-200% 范围内,表明无明显干扰;若回收率异常,需通过过滤、中和、透析、加热处理等方式优化样品前处理。方法学确认还需涵盖线性范围(如 0.005-5 EU/mL)、精密度(批内 CV≤15%)、检测限(LOD≤0.01 EU/mL)等指标,确保方法在实际样品检测中稳定可靠,符合《美国药典》 <85>、《中国药典》通则 1143 等药典要求。
细菌内毒素检查法用鲎试剂检测或量化革兰阴性菌内毒素,判断供试品限量是否合规。江苏抗体药物内毒素检测抗干扰方案
内毒素检测复孔 CV>15%,需校准移液枪,规范加样,排查耗材污染。北京化学制药内毒素检测动态显色法鲎试剂
内毒素检测常与热原检测混淆,二者既有关联又有区别:热原是指所有能引起发热的物质(包括内毒素、病毒、真菌等),通过传统家兔热原试验检测;内毒素是热原的主要成分(占 90% 以上),检测更具特异性。目前,家兔热原试验因操作复杂、动物成本高,已逐渐被单核细胞活化反应测定法(MAT)替代,但部分产品(如放射性质药物、血液制品)仍需保留家兔试验作为补充。法规要求内毒素检测结果需与热原风险关联,若内毒素检测合格但临床出现热原反应,需排查是否存在非内毒素类热原,通过联合检测确保产品安全性。
北京化学制药内毒素检测动态显色法鲎试剂