大肠杆菌具有遗传性状清晰,易于培养和控制,表达水平高,成本低,周期短等特点,是优先的经济实惠的蛋白表达系统,K-12系列和B系列菌株是工业规模上常用于生物工程的E.coli细菌株。K-12菌种、所衍生出的DH5α、Top10、JM109等菌株,可用于大量生产质粒DNA并进一步制备细胞基因治疗产品和病毒载体类疫苗。源于B系的菌株,如BL21,更适用于高效转染表达载体和常规蛋白的表达,如:病毒蛋白、重组蛋白疫苗、细胞因子、酶类等产品。湖州申科生物针对这两种菌株的特点,分别开发了E.coli表达菌HCP残留检测试剂盒和E.coli克隆菌碱裂HCP残留检测试剂盒。
湖州申科开发多种宿主 HCP 检测试剂盒,提供抗体覆盖率验证服务。CHO-K1宿主细胞蛋白(HCP)残留检测桥接验证
湖州申科生物CHO-K1 HCP 残留检测试剂盒(一步酶联免疫吸附法)基于固相酶联免疫吸附分析法,适用于基于CHO-K1细胞生产的生物制品中宿主残留蛋白的定量检测。该分析方法通过在预包被抗CHO-K1HCPs绵羊多抗的酶标板中加入校准品或待测样品、HRP标记的抗CHO-K1HCPs绵羊多抗进行共孵育。洗涤后,加入TMB底物进行显色反应,再使用终止液终止酶催化反应。利用酶标仪在450nm波长下测读吸光度,其吸光度与校准品或待测样品中的HCPs浓度成正相关,通过校准品拟合的剂量-反应曲线即可计算得出待测样品中HCPs的浓度。本试剂盒对待测样品无需进行特殊处理,只需通过合适的稀释比例进行适用性验证即可直接使用。本试剂盒操作步骤少,快速,检测专一性强,性能稳定可靠。
CHO-K1宿主细胞蛋白(HCP)残留检测桥接验证部分数据表明,定制化HCP检测试剂盒的检测准确度比商业化试剂盒高,更能满足产品质量控制所需。
全球快速增长的抗体、蛋白类药物等生物药由相应工程细胞生产。生物制品药物生产过程中的宿主内源性蛋白,被称为宿主细胞蛋白(Host Cell Proteins, HCPs)会随着不同工艺流程部分残留在药物中。宿主细胞残留蛋白作为外源蛋白可能会在不同程度上引发机体的免疫应答,导致过敏反应或其它不良反应;另外还有一些残留HCPs具有蛋白酶或脂酶的活性,可能导致蛋白药物或辅料的降解,进而增加药物产品的质量和疗效的不稳定性。基于此,对药物中HCPs的定性与定量检测就显得尤为重要。全球各国药典如美国药典,欧洲药典以及中国药典都对HCPs检测提出了具体要求和标准。
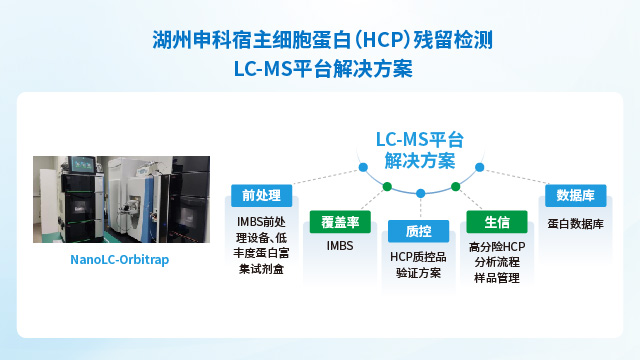
美国药典USP通则<1132.1> Residual Host Cell Protein Measurement in Biopharmaceuticals by Mass Spectrometry(质谱法测定生物药中残留宿主细胞蛋白)主要介绍了LC-MS技术在宿主细胞残留蛋白检测中的应用,从样品制备、质谱测试条件的建立、数据的分析、质谱方法验证等多个方面,详细阐述了质谱技术在HCPs中应用的优势与注意事项。作为一种先进的分析技术平台,质谱技术在HCPs分析中的应用,以及与ELISA方法和其他分析方法结合使用,有助于生产企业在产品的整个生命周期中更好地理解和建立HCPs的检测方法,保证产品质量的稳定。
工艺特异型试剂盒针对特定生产流程,准确监控HCP残留,适配工艺变动。
大肠埃希氏菌(Escherichia coli,E. coli )又称大肠杆菌,其作为模式微生物被广泛应用于生命科学研究中。大肠杆菌是表达药用异源蛋白的常用微生物,在被批准的药用蛋白中,大约30%的产品以大肠杆菌作为表达宿主菌。与其他表达平台一样,尽管下游复杂的纯化步骤已经去除了大量的杂质,但终产品中仍会存在HCP残留风险,必须对其进行质量控制,使其符合放行标准。湖州申科生物E.coli表达菌HCP残留检测试剂盒用于大肠杆菌表达菌株BL21来源的宿主细胞蛋白定量检测,适用于重组蛋白类产品的工艺中间品和原液类样品,如白细胞介素(IL)、干扰素(rhIFN)、粒细胞-巨噬细胞集落刺激因子(rhGM-CSF)、肿瘤坏死因子(rhTNF)、促生长因子(EGF/FGF/PDGF)等。试剂盒检测步骤少,快速,专一性强,性能稳定可靠。
湖州申科系列HCP检测产品均进行了校准品的表征分析,抗体覆盖率分析。上海ELISA法宿主细胞蛋白(HCP)残留检测免疫策略
临床 III 期及商业化生产阶段,法规推荐用定制化 HCP ELISA 试剂盒保障检测针对性。CHO-K1宿主细胞蛋白(HCP)残留检测桥接验证
影响宿主细胞蛋白(HCP)残留检测结果的因素之一是操作规范。一方面,实验人员的专业技能和经验对检测结果的准确性有很大影响。熟练的实验人员能够准确地进行样品处理、试剂配制和仪器操作,减少人为误差。另一方面,一个合理的HCP检测方法,在开发及应用时,应当考虑操作的合理变动区间(即耐用性)并设置相质控,从程序上尽量消除人为误差对结果的影响。此外,严格遵循标准操作流程(SOP)是确保检测结果可靠性的关键。操作步骤的不规范可能导致结果的重复性差或误差增大。目前,湖州申科已正式推出全自动化HCP ELISA检测系统,可以完成从样品制备、孵育、洗板至数据采集等一系列操作,结合实验室信息管理系统(LIMS),可以实现“输入即输出”,减少流程误差。
CHO-K1宿主细胞蛋白(HCP)残留检测桥接验证