-
 广东生物制品宿主细胞残留DNA检测10.04
广东生物制品宿主细胞残留DNA检测10.04SHENTEK® PG13 残留 DNA 检测试剂盒,可对各类生物制品的中间品、半成品及成品中 PG13 宿主细胞 DNA 进行定量检测分析。该试剂盒基于 PCR 荧光探针法原理,实现对样品中 P...

-
 安徽qPCR法宿主细胞残留DNA检测方案10.04
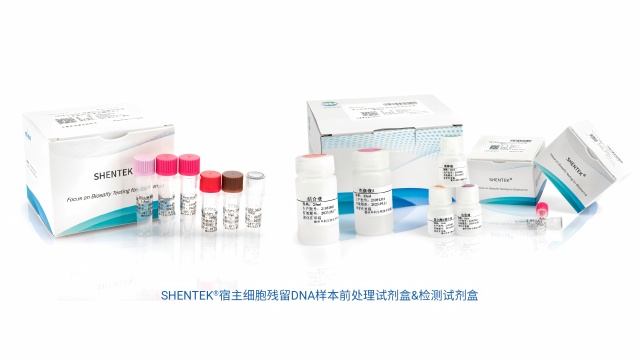
安徽qPCR法宿主细胞残留DNA检测方案10.04宿主细胞残留DNA样本前处理试剂盒(磁珠法)机装版,适用于生物制品样品前处理,能稳定高效获取样品中的微量宿主细胞DNA。该试剂盒可在多种复杂基质缓冲液(如细胞裂解液、澄清上清、纯化中间品等)中,实...

-
 湖北生物制品宿主细胞残留DNA检测生产企业10.04
湖北生物制品宿主细胞残留DNA检测生产企业10.04美国食品药品监督管理局(FDA)提示,采用 HEK293T 细胞生产病毒载体时,因该细胞中存在 SV40 T 抗原,还需额外检测残留的腺病毒 E1(E1A 与 E1B)及 SV40 T 抗原序列。...

-
 甘肃Vero宿主细胞残留DNA检测常用知识10.04
甘肃Vero宿主细胞残留DNA检测常用知识10.04美国食品药品监督管理局(FDA)提示,采用 HEK293T 细胞生产病毒载体时,因该细胞中存在 SV40 T 抗原,还需额外检测残留的腺病毒 E1(E1A 与 E1B)及 SV40 T 抗原序列。...

-
 上海CHO宿主细胞残留DNA检测常见问题10.04
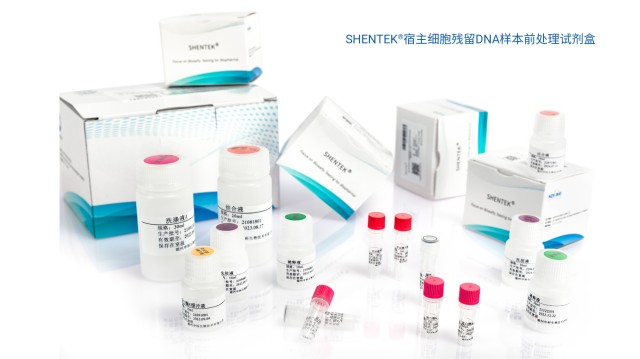
上海CHO宿主细胞残留DNA检测常见问题10.04生物制品宿主细胞残留 DNA 检测是生物制药领域的关键质量控制环节,主要目的是定量监测疫苗、单抗、基因治疗产品等生物制品中宿主细胞来源的 DNA 残留量,以此评估潜在安全风险并确保符合法规要求。其...

-
 广东化学制药内毒素检测技术升级10.03
广东化学制药内毒素检测技术升级10.03生物制品(如单抗、疫苗、重组蛋白)注射剂因直接进入人体,对细菌内毒素残留限值要求严苛(通常≤0.5 EU/mg 或更低),检测面临基质复杂、干扰物质多等挑战。样品中常见的蛋白质、螯合剂、表面活性剂...

-
 上海热原检测操作步骤10.03
上海热原检测操作步骤10.03MAT法(单核细胞活化反应测定)热原检测基于人体免疫反应机制设计,原理是:内毒素(革兰氏阴性菌来源)与非内毒素热原(革兰氏阳性菌、霉菌、病毒等来源)进入人体后,会活化单核细胞或单核细胞系,使其释放...

-
 四川qPCR法宿主细胞残留DNA检测常见问题10.03
四川qPCR法宿主细胞残留DNA检测常见问题10.03重组蛋白、抗体、疫苗、细胞与基因类生物制品,大多源自细菌、酵母、动物或人源细胞等生物工程细胞构成的复杂表达/生产系统。不同宿主对应的rHCD与rHCR存在差异,且二者具有不同片段长度与组成的复杂阵...

-
 安徽宿主细胞残留DNA检测方案10.03
安徽宿主细胞残留DNA检测方案10.03SHENTEK® 毕赤酵母残留 DNA 检测试剂盒,可对各类生物制品及药品的中间品、半成品与成品中,毕赤酵母宿主细胞 DNA 进行定量检测。该试剂盒基于荧光探针法原理,实现对样品中毕赤酵母残留 DNA...

-
 江西qPCR法宿主细胞残留DNA检测10.03
江西qPCR法宿主细胞残留DNA检测10.03宿主细胞残留DNA的潜在风险中,传播性是其中一项。该风险源于残留DNA可能携带带有潜在入侵能力的完整或部分病毒基因组序列,这类序列主要有两大来源:1)整合到宿主基因组中的DNA病毒序列,或是染色体...

-
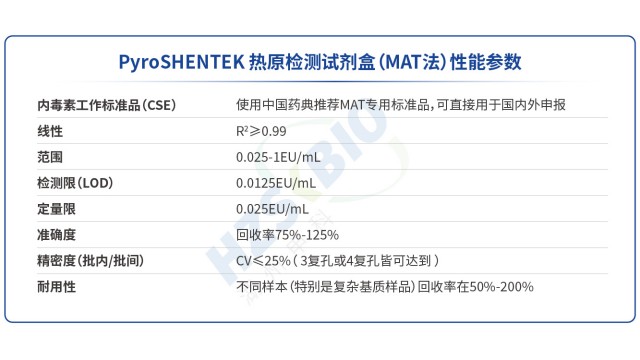 血液制品热原检测常见问题分析10.03
血液制品热原检测常见问题分析10.03单核细胞系凭借标准化、可控性等优势,有效解决PBMC(外周血单个核细胞)在热原检测中的局限。其一,单核细胞系源自永生化细胞株(如 Mono-Mac-6),经筛选后细胞特性高度均一,消除供体差异,让...

-
 上海细菌内毒素检测结果判定10.03
上海细菌内毒素检测结果判定10.03重组级联试剂作为内毒素检测鲎试剂的理想替代方案,其具备的优势有:①优化的G因子级联反应,无G因子旁路干扰。采用基因重组技术表达鲎血细胞中的C因子(Factor C)、B因子(Factor B)和凝...
