-
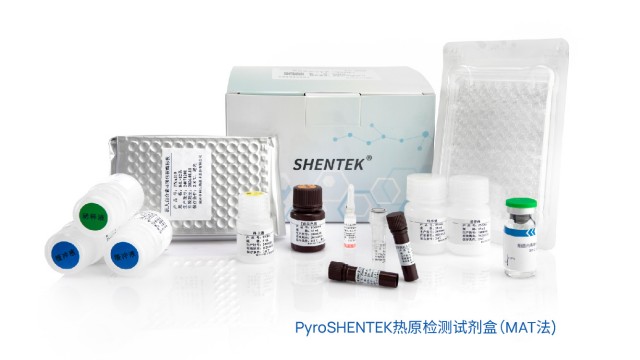 北京化学制药热原检测流程10.07
北京化学制药热原检测流程10.07MAT 试剂盒配套的即用型细胞存在明确的传代限制,且商业化传代需获得授权,关键是保障细胞质量与检测可靠性。首先,即用型细胞经特殊工艺优化,已处于较好的活性与热原响应状态,不适合传代,传代后细胞会出...

-
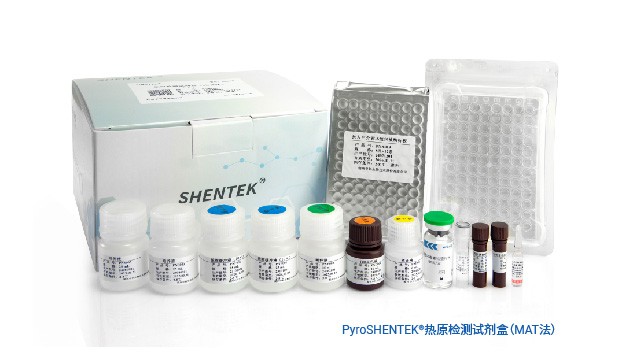 山东热原检测家兔法替代方案10.07
山东热原检测家兔法替代方案10.07中国药典对 MAT 法热原检测要求 4 复孔,未明确 CV 限值,需结合细胞实验特性合理解读与操作。药典不设 CV 限值的主要原因是:MAT 法基于细胞反应,细胞活性易受环境微小变化(如温度、pH...

-
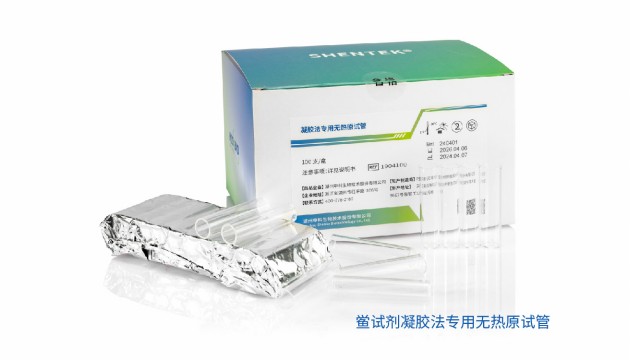 广东医疗器械内毒素检测风险评估10.07
广东医疗器械内毒素检测风险评估10.07血液制品(如白蛋白、免疫球蛋白、凝血因子)来源于人血浆,内毒素污染风险高,且基质中含大量蛋白质、脂质等干扰物质,检测难度较大。传统 LAL 法易受血浆蛋白抑制,需通过预处理去除干扰:如采用三氯乙酸...

-
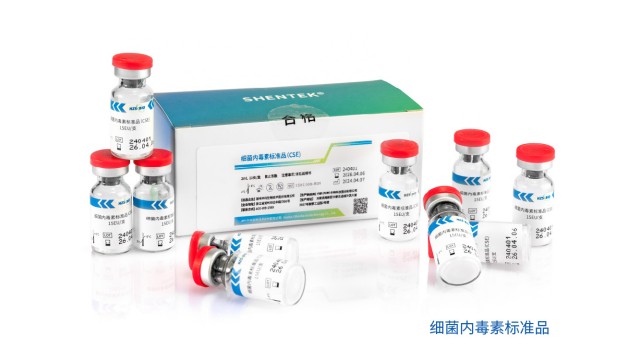 重组蛋白内毒素检测低内毒素回收10.07
重组蛋白内毒素检测低内毒素回收10.07如何准备样品进行内毒素检测呢?测试前,需要根据样品实际情况进行样本前处理。大多数样品只需要稀释,使用内毒素检测试剂盒进行测试即可。如果样品有蛋白酶干扰并导致假阳性结果,建议对样品稀释并70°C加热...

-
 浙江内毒素检测技术服务10.06
浙江内毒素检测技术服务10.06内毒素检测结果误差可能源于多环节:试剂方面,鲎试剂(LAL )或试剂批间差异、过期试剂活性下降会导致结果偏差,需通过试剂验收(如阳性对照回收率验证)确保质量;操作方面,实验器具未除热原(如玻璃器皿...

-
 辽宁Vero宿主细胞残留DNA检测10.06
辽宁Vero宿主细胞残留DNA检测10.06SHENTEK®NS0&SP2/0残留DNA检测试剂盒,可对各类生物制品及药品的中间品、半成品与成品中NS0或SP2/0宿主细胞DNA进行定量检测。该试剂盒基于荧光探针法原理,实现对样品中NS0或...

-
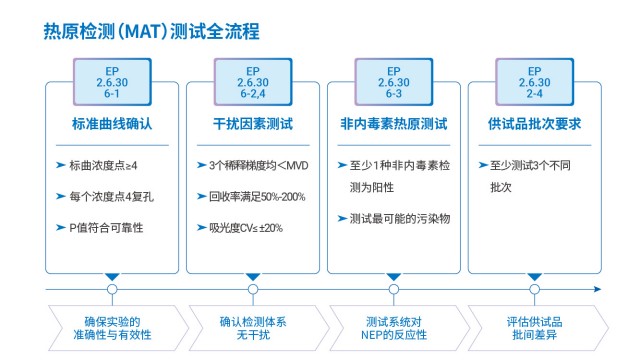 四川热原检测操作步骤10.06
四川热原检测操作步骤10.06PyroSHENTEK®热原检测试剂盒依据 ICH Q2 (R2)、《中国药典》(如通则 9301)及欧洲药典(EP 2.6.30)要求,完成了线性、范围、定量限、准确度、精密度、耐用性等全维度性...

-
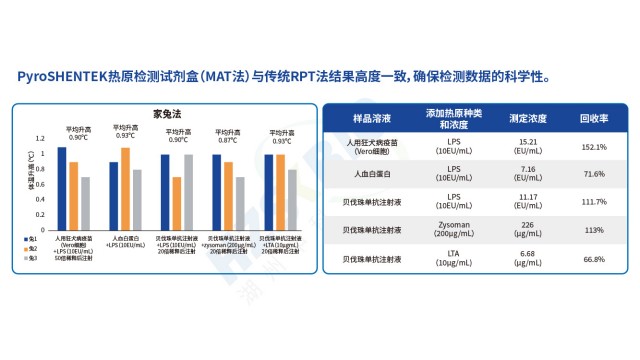 江苏高效热原检测风险评估10.06
江苏高效热原检测风险评估10.06随着发热反应分子机制研究的不断深化,单核细胞活化试验(MAT)作为一种体外热原检测技术,愈发受到医药与医疗器械行业的关注并逐步推广应用。该方法的原理是:让人体全血与待检样品中的热原充分接触后,通过...

-
 北京细菌内毒素检测常见问题分析10.06
北京细菌内毒素检测常见问题分析10.06湖州申科生物凝胶法鲎试剂凭借合规性和实用性,成为实验室内毒素定量检测的优先选择。该产品严格符合 USP、EP、中国药典标准,提供 0.03、0.06、0.125、0.25、0.5EU/mL 等多种...

-
 上海医疗器械内毒素检测常见问题分析10.06
上海医疗器械内毒素检测常见问题分析10.06内毒素检测常与热原检测混淆,二者既有关联又有区别:热原是指所有能引起发热的物质(包括内毒素、病毒、真菌等),通过传统家兔热原试验检测;内毒素是热原的主要成分(占 90% 以上),检测更具特异性。目...

-
 吉林qPCR法宿主细胞残留DNA检测常用知识10.06
吉林qPCR法宿主细胞残留DNA检测常用知识10.06MDCK 细胞作为宿主工程用细胞,其宿主细胞DNA残留会给机体带来安全风险。虽然 MDCK 细胞基质流感疫苗生产中,已采用超滤、核酸酶处理、层析、β- 丙内酯灭活等工艺去除残留 DNA,但疫苗产品里仍...

-
 重组蛋白内毒素检测重组级联试剂(rCR)10.05
重组蛋白内毒素检测重组级联试剂(rCR)10.05生物制品(如单抗、疫苗、重组蛋白)注射剂因直接进入人体,对细菌内毒素残留限值要求严苛(通常≤0.5 EU/mg 或更低),检测面临基质复杂、干扰物质多等挑战。样品中常见的蛋白质、螯合剂、表面活性剂...
