- 产地
- 苏州
- 品牌
- 外泌体提取试剂
- 型号
- 齐全
- 是否定制
- 是
外泌体不断地被细胞产生和吸收。它们可能是新生成的外泌体和消耗的外泌体的混合物(红色和蓝色)。目前尚不清楚内生性产生或消耗的外泌体是一起释放还是单独释放。外泌体与生殖发育,抗细菌:人类的生殖,妊娠和胚胎发育需要精确,微调和动态的细胞间通讯。**,羊水,血液和母乳均含有具有特定功能的外泌体:精浆来源的外泌体与生殖器免疫有关,还有助于阻断HIV的传染;胎盘滋养细胞来源的外泌体可将一类miRNA输送至非胎盘细胞,促进自噬和细菌防御机能;母乳来源的外泌体也对婴儿的免疫系统有帮助。使用可截留100KD分子量的膜,通过离心截留上清中的外泌体,截留完成后。上海外泌体提取试剂厂家现货

外泌体在肺病进程中的作用:肺病细胞来源外泌体(LCC-exosome)可以通过刺激一些病症血管的形成来促进一些病症的生长。据相关报道称,LCC-exosome中的miR-210可以通过调节基质细胞中酪氨酸受体激酶A3的含量,促进一些病症血管的生成;而LCC-exosome中的miR-23a则可以通过启动脯氨酰羟化酶及压制紧密结合蛋白ZO-1来促进肺病的生血管作用。此外,有研究发现,外泌体中的内容物可以触发上皮-间质转化(EMT)。晚期肺病患者血清中外泌体波形蛋白表达增加,促使人正常支气管上皮细胞出现EMT,从而使肺支气管正常上皮细胞出现增殖,迁移能力。杭州正规外泌体提取试剂厂家获得的外泌体纯度较高,但步骤繁琐,耗时。

人体内多种细胞及体液均可分泌外泌体,包括内皮细胞、免疫细胞、血小板、平滑肌细胞等。当其由宿主细胞被分泌到受体细胞中时,外泌体可通过其携带的蛋白质、核酸、脂类等来调节受体细胞的生物学活性。外泌体介导的细胞间通讯主要通过以下三种方式:一是外泌体膜蛋白可以与靶细胞膜蛋白结合,进而启动靶细胞细胞内的信号通路。二是在细胞外基质中,外泌体膜蛋白可以被蛋白酶剪切,剪切的碎片可以作为配体与细胞膜上的受体结合,从而启动细胞内的信号通路。有报道称一些外泌体膜上蛋白在其来源细胞膜上未能检测出。三是外泌体膜可以与靶细胞膜直接融合,非选择性的释放其所含的蛋白质、mRNA以及microRNA。
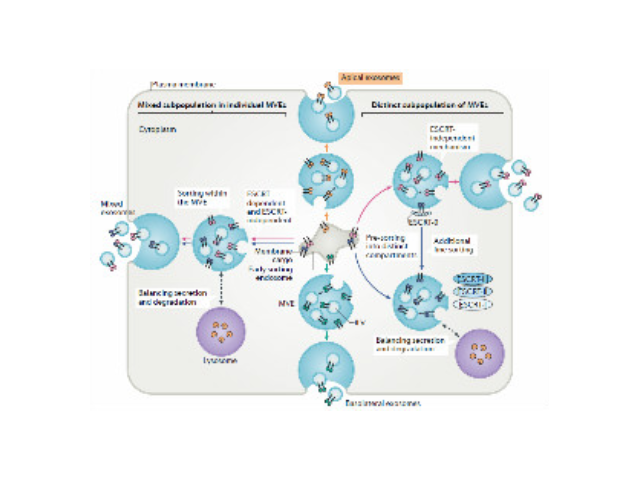
2015年,随着精细医学概念的提出,越来越多的人开始关注如何能做到疾病的精确诊断和治病。外泌体作为一个新型的研究热点,由于它在体内存在的普遍性和获取的便捷性,已经成为了疾病诊断治病的潜在有效方式,在精细医学发展上有着光明的前景。多泡内体的腔内囊泡,要么分选进溶酶体将物质降解,要么作为外泌体分泌到胞外环境中。将膜分选到不同的腔内囊泡群中的机制尚不清楚。该研究发现物质被分选到内体膜上的不同子域中,并且外泌体相关结构域向内体腔的转移不取决于ESCRT(运输所需的内体分选复合体)的功能,但是需要鞘脂神经酰胺。纯化的外体富含神经酰胺,并且在神经鞘磷脂酶被压制后外泌体释放减少。这些结果确定了内体内膜运输和外泌体形成的途径。外泌体生物活性易受pH和盐浓度影响,不利于下游实验,难以普遍普及。

外泌体的提取的方式:1、免疫磁珠法,这种方法可以保证外泌体形态的完整,特异性高、操作简单、不需要昂贵的仪器设备,但是非中性pH和非生理性盐浓度会影响外泌体生物活性,不便进行下一步的实验。2、PS亲和法,该方法将PS(磷脂酰丝氨酸)与磁珠结合,利用亲和原理捕获外泌体囊泡外的PS。该方法与免疫磁珠法相似,获得的外泌体形态完整,纯度较高。由于不使用变性剂,不影响外泌体的生物活性,外泌体可用于细胞共培养和体内注射。2016.9《ScientificReports》杂志发表了该方法较新数据,表明PS法可提取相当高纯度的外泌体。六是色谱法,这种方法分离到的外泌体在电镜下大小均一,但是需要特殊的设备,应用不普遍。超滤离心法简单高效,且不影响外泌体的生物活性,但同样存在纯度不高的问题。合肥正规外泌体提取试剂厂家供应
将沉淀物用PBS缓冲液进行悬浮,使外泌体悬浮于液体上层。上海外泌体提取试剂厂家现货
1983年,外泌体初次于绵羊网织红细胞中被发现,1987年Johnstone将其命名为“exosome”。多种细胞在正常及病理状态下均可分泌外泌体。其主要来源于细胞内溶酶体微粒内陷形成的多囊泡体,经多囊泡体外膜与细胞膜融合后释放到胞外基质中。所有培养的细胞类型均可分泌外泌体,且外泌体天然存在于体液中,包括血液、唾液、尿液、脑脊液和乳汁中。有关他们分泌和摄取及其组成、“运载物”和相应功能的精确分子机制刚刚开始研究。外泌体目前被视为特异性分泌的膜泡,参与细胞间通讯,对外泌体的研究兴趣日益增长,无论是研究其功能还是了解如何将其用于微创诊断的开发。上海外泌体提取试剂厂家现货
外泌体的提取方法:1.超速离心法(差速离心)。超离法是较常用的外泌体纯化手段,采用低速离心、高速离心交替进行,可分离到大小相近的囊泡颗粒。超离法因操作简单,获得的囊泡数量较多而广受欢迎,但过程比较费时,且回收率不稳定(可能与转子类型有关),纯度也受到质疑;此外,重复离心操作还有可能对囊泡造成损害,从而降低其质量。2.密度梯度离心。在超速离心力作用下,使蔗糖溶液形成从低到高连续分布的密度阶层,是一种区带分离法。通过密度梯度离心,样品中的外泌体将在1.13-1.19g/ml的密度范围富集。此法获得的外泌体纯度较高,但步骤繁琐,耗时,对离心时间极为敏感。此提取方法条件复杂,成本高。昆明正规外泌体提取...
- 成都正规外泌体提取试剂 2026-05-24
- 重庆正规外泌体提取试剂哪家便宜 2026-05-24
- 芜湖外泌体提取试剂厂家现货 2026-05-24
- 正规外泌体提取试剂供应商 2026-05-24
- 南京正规外泌体提取试剂厂家供应 2026-05-23
- 宁波外泌体提取试剂厂家批发价 2026-05-23
- 广州正规外泌体提取试剂推荐厂家 2026-05-23
- 贵阳正规外泌体提取试剂报价 2026-05-22
- 南昌正规外泌体提取试剂 2026-05-22
- 天津正规外泌体提取试剂直销价 2026-05-22
- 天津正规外泌体提取试剂厂家 2026-05-17
- 南昌正规外泌体提取试剂哪里买 2026-05-16
- 成都正规外泌体提取试剂价格 2026-05-16
- 芜湖正规外泌体提取试剂厂家供应 2026-05-15
- 合肥外泌体提取试剂推荐厂家 2026-05-14
- 石家庄正规外泌体提取试剂厂家 2026-05-14


- 口碑好的糖原染色试剂盒进货价 05-24
- 北京RNA提取试剂厂家 05-24
- 济南细胞外基质胶单价 05-24
- 珠海RNA提取试剂厂家推荐 05-24
- 重庆无血清细胞冻存液直销厂家 05-24
- 芜湖唐山RNA提取试剂 05-24
- 哪家生产糖原染色试剂盒厂家批发价 05-24
- 南昌正规无血清细胞冻存液销售厂家 05-24
- 无锡RNA提取试剂哪家好 05-24
- 南京原代细胞分离试剂盒哪家便宜 05-24