- 品牌
- 苏心
- 型号
- 齐全
根据剂量和结构,干粉吸入器可分为以下三类:单剂量型**产品:噻托溴铵粉吸入剂(思力华)、天晴速乐。特点:每次使用需装入单剂量胶囊,通过旋转或刺破胶囊释放药物。适用于慢性阻塞性肺疾病的维持***,可避免药物浪费。多剂量型**产品:***替卡松粉吸入剂(舒利迭)。特点:药物以泡罩或箔片形式密封,通过拨动滑动杆释放单次剂量。操作简便,适合长期使用,尤其适用于***患者。储存剂量型**产品:布地奈德福莫特罗粉吸入剂(信必可都保)、普米克都保。呼气:轻轻呼出一口气(避免对吸嘴吹气)。太仓特色干粉吸入器客服电话

1、噻托溴铵作为每日一次维持***的支气管扩张药,不应用作支气管痉挛急性发作的初始***,即抢救***药物。2、在吸入噻托溴铵粉末后有可能立即发生过敏反应。3、与其它抗胆碱能药物一样,对于窄角型青光眼、前列腺增生、或膀胱颈梗阻的患者应谨慎使用。4、吸入药物可能引起吸入性支气管痉挛。5、与所有主要经肾脏排泄的药物一样,对于中、重度肾功能不全(肌酐***率≤50ml/min)的患者,只有在预期利益大于可能产生的危害时,才能使用噻托溴铵。尚无严重肾功能不全患者长期使用噻托溴铵的经验。工业园区服务干粉吸入器工厂直销每次使用需装入单剂量胶囊,通过旋转或刺破胶囊释放药物。

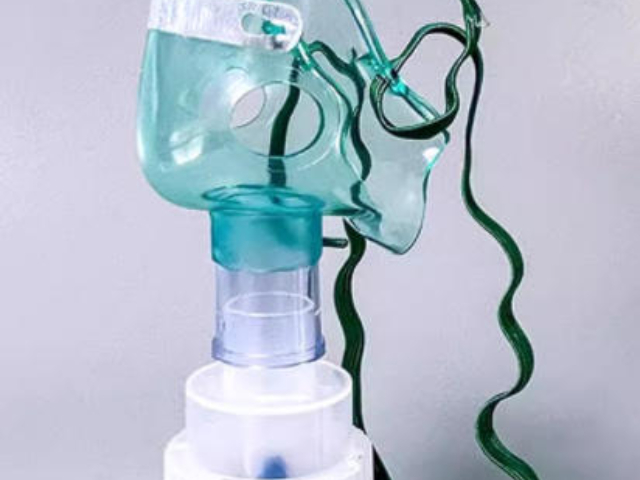
吸入器是一种用于将药物直接送入呼吸道的医疗设备,常用于******、慢性阻塞性肺病(COPD)等呼吸系统疾病。吸入器的主要类型包括:定量吸入器(MDI):这种吸入器通常是一个小型的气雾剂,使用时需要配合吸气,能够精确控制每次吸入的药物剂量。干粉吸入器(DPI):这种吸入器通过吸入空气来***药物,药物以干粉形式存在,使用时需要用力吸气。雾化器:将液体药物转化为细小的雾状颗粒,患者通过面罩或嘴巴吸入,适合于小孩或重症患者。
雾化器:连接面罩或口含器,正常呼吸即可。清洁与保养:定期清洗喷嘴或面罩,避免药物残留。存放于干燥、避光处,避免高温或潮湿。四、吸入器的优缺点优点:药物直接作用于靶***,起效快,副作用少。便携性强,适合长期使用。缺点:部分患者操作困难(如pMDI需协调动作)。干粉吸入器依赖吸气力度,儿童或老人可能使用受限。雾化器需电源,不适合紧急情况。五、常见问题与注意事项操作错误:未屏气或吸气过快可能导致药物沉积在口腔而非肺部。解决方案:通过示范或视频学习正确技巧。药物残留:雾化器未清洁可能导致细菌滋生。布地奈德福莫特罗粉吸入剂(信必可都保)、普米克都保。

如有出现肾上腺功能不全的征象,应暂时增加其全身糖皮质***剂量,然后继续更慢地撤除。在应激时期或严重***发作时,改用吸入的患者需要补充全身***。若使用超过推荐剂量的普米克都保,其安全性和有效性尚未确定。慢性阻塞性肺病(COPD) 普米克都保的推荐剂量是400 ug,1日2次。口服糖皮质***的COPD患者,若减少口服剂量,其普米克都保的用量应和用法用量;“支气管***”的推荐剂量相同。说明:本干粉吸入剂为白色至灰白色圆形颗粒,轻压后成为粉末状,填入特制的吸入气流驱动的多剂量粉末吸入器中计数装置:关注剩余药量,及时更换装置。太仓特色干粉吸入器客服电话
充填药物:一手握吸入器,另一手旋转底盖至听到“咔嗒”声,完成单次剂量充填。太仓特色干粉吸入器客服电话
这种作用具有竞争性和可逆性。体内、体外研究显示本品具有剂量依赖性的、可持续 24h的抑制乙酰甲胆碱诱导的支气管收缩作用。本品对支气管的扩张作用具有突出的定位选择性。毒理研究生殖毒性:大鼠吸入剂量达1.689mg/kg /d(按体表面积计算,约为临床推荐日剂量的760倍),对生育力未见影响。大鼠吸入剂量达0.078mg/kg/d(按体表面积计算,约为临床推荐日剂量的35倍),有流产,活胎数量和平均胎儿重量减少,胎儿的性成熟延迟的作用;兔吸入剂量达0.4mg/kg/d(按体表面积计算,约为临床推荐日剂量的 360倍),增加植入后的丢失。太仓特色干粉吸入器客服电话
苏心微医学科技(苏州)有限公司汇集了大量的优秀人才,集企业奇思,创经济奇迹,一群有梦想有朝气的团队不断在前进的道路上开创新天地,绘画新蓝图,在江苏省等地区的医药健康中始终保持良好的信誉,信奉着“争取每一个客户不容易,失去每一个用户很简单”的理念,市场是企业的方向,质量是企业的生命,在公司有效方针的领导下,全体上下,团结一致,共同进退,**协力把各方面工作做得更好,努力开创工作的新局面,公司的新高度,未来苏心供应和您一起奔向更美好的未来,即使现在有一点小小的成绩,也不足以骄傲,过去的种种都已成为昨日我们只有总结经验,才能继续上路,让我们一起点燃新的希望,放飞新的梦想!
液体吸入剂液体吸入剂的关键是保证较高的药物肺部沉积率。美国爱罗金公司拥有新颖的液体气雾剂**技术,特点是小巧、轻便和无抛射剂。此电子控制液体气雾剂给药器被开发成两种特殊的产品,其中Aero Dose为单剂或多剂液体吸入剂,用于肺部释放一系列呼吸系统药物、蛋白质和肽类药物,有较高的下呼吸道或肺深部沉积率,释放大分子药物优于其他肺部释药新技术(如干粉吸入剂),可降低单位剂量的费用、提高剂量的准确性和蛋白质的稳定性;Aero Neb为无噪音、轻便和易携带的喷雾剂,可稳定喷散释放出大小一致的小药滴,美国FDA已批准了此给药器具。便携性:通常体积小,易于携带,适合日常使用。苏州服务干粉吸入器电话多少但在...
- 工业园区质量干粉吸入器销售厂家 2026-05-03
- 工业园区名优干粉吸入器工厂直销 2026-05-03
- 常熟现代干粉吸入器客服电话 2026-05-03
- 江苏本地干粉吸入器生产企业 2026-05-02
- 江苏服务干粉吸入器价位 2026-05-02
- 工业园区特色干粉吸入器专卖店 2026-05-02
- 吴江区现代干粉吸入器销售厂家 2026-05-02
- 吴中区现代干粉吸入器销售厂家 2026-05-02
- 吴江区标准干粉吸入器价位 2026-05-02
- 工业园区本地干粉吸入器销售厂家 2026-05-02
- 相城区特色干粉吸入器客服电话 2026-05-02
- 吴江区标准干粉吸入器24小时服务 2026-05-02
- 姑苏区名优干粉吸入器工厂直销 2026-05-02
- 常熟标准干粉吸入器24小时服务 2026-05-02
- 高新区名优干粉吸入器服务热线 2026-05-02
- 高新区服务干粉吸入器电话多少 2026-05-02


- 工业园区名优干粉吸入器工厂直销 05-03
- 江苏现代软雾吸入器电话多少 05-03
- 常熟质量软雾吸入器厂家电话 05-03
- 常熟现代干粉吸入器客服电话 05-03
- 常熟现代软雾吸入器价位 05-03
- 姑苏区名优软雾吸入器工厂直销 05-03
- 工业园区质量软雾吸入器24小时服务 05-02
- 江苏本地干粉吸入器生产企业 05-02
- 江苏服务干粉吸入器价位 05-02
- 虎丘区特色软雾吸入器价位 05-02