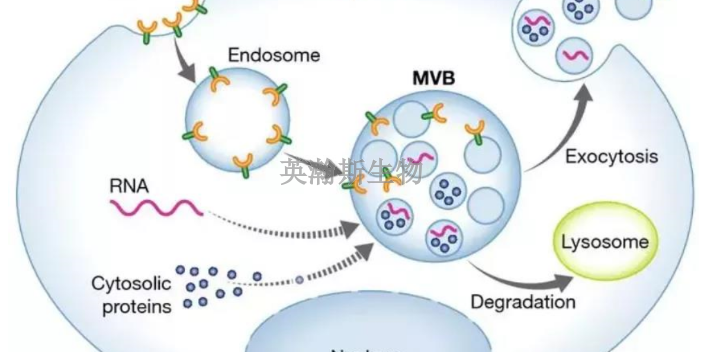
外泌体是所有细胞产生的胞外小泡,携带核酸、蛋白质、脂质和代谢物。它们是健康和疾病中细胞间近距离通讯的介质,影响细胞生物学的各个方面。外泌体的生物发生 细胞质膜内陷,将一些细胞外成分和细胞膜蛋白包裹在一起,形成早期内涵体(ESEs),这些ESEs可以与其他细胞器发生物质交换,或者不同ESEs之间融合形成晚期内涵体(LSEs),进一步形成细胞内多膜体(MVBs),其中会包含许多腔内囊泡(ILVs),这些ILVs将来就可能会被释放成为外泌体。外泌体在分泌细胞和受体细胞间的穿梭介导了细胞间的生物分子传递。山东专门做外泌体检测
外泌体不仅*是一种物理载体,还在分子生物学层面上发挥着重要作用,尤其是微RNA(miRNA)的转运。微RNA是一类小型的非编码RNA,能够调控基因表达,在细胞的多种生理过程中发挥重要作用。研究发现,外泌体中含有大量miRNA,并且这些miRNA可以通过外泌体在不同细胞间进行传递,从而影响目标细胞的基因表达。例如,外泌体中的miRNA能够调控**的发生和发展,影响细胞的增殖、迁移和侵袭。外泌体作为miRNA的载体,不仅有助于miRNA的稳定性,还能保证其在细胞间的有效传递。通过这种方式,外泌体能够在体内的细胞间传播基因表达调控信息。因此,外泌体和miRNA的关系为我们提供了一个全新的理解细胞间通信的视角,并为开发新的***策略提供了理论基础。浙江推荐的外泌体外泌体研究整体解决方案_英瀚斯生物。
尽管外泌体研究进展迅速,但其商业化和临床转化仍面临诸多挑战。首要问题是分离纯化方法尚未标准化,不同实验室采用不同提取手段,可能导致结果不一致。其次,外泌体成分复杂且受来源细胞状态影响较大,缺乏统一的质量控制标准。此外,如何实现大规模制备、长效保存及安全性评估也是目前研究的热点。监管方面,目前尚无针对外泌体类产品的完整法规体系,特别是在***用途方面,急需建立从实验室研究到临床应用的桥梁。未来的发展需依赖多学科交叉融合,包括材料学、生物工程、药代动力学等方向的深度参与。
外泌体的生成,微泡是由质膜的出芽形成的,膜双层通过磷脂的不对称分布来维持脂质的“多面性”。外层富含磷脂酰胆碱和鞘磷脂,而内层主要由磷脂酰丝氨酸和磷脂酰乙醇胺形成。然而,胞质Ca2+的内流可以破坏这种不对称性,导致磷脂跨膜双层的重新分配,促进膜起泡。依赖Ca2+的蛋白水解同时降解膜相关的细胞骨架,促进出芽过程。在外泌体形成过程中,首先,MVE(多囊体)向内芽形成小泡,内含来自细胞质的货物(蛋白质、mRNA和miRNAs)。然后,MVE要么与细胞膜融合释放外泌体(内囊泡),要么与溶酶体融合降解MVE含量。到达目的地后,外泌体通过内吞途径或与靶细胞膜融合,将其内容物释放到细胞质中。细胞的膜的囊泡也可以直接从细胞膜上萌发,携带活性蛋白、RNA和其他化合物。外泌体提取,超离法是比较常用的外泌体纯化手段。
干细胞外泌体在再生医学中展现出***优势,逐渐成为细胞***之外的一种替代策略。间充质干细胞(MSC)因其免疫原性低、生物活性强而广泛应用于组织修复,而研究发现其外泌体也具备类似的修复功能。例如,MSC外泌体可促进血管生成、抑制凋亡、调节炎症,并已在心肌梗死、肝损伤、肾衰等动物模型中展现良好疗效。与干细胞相比,外泌体的储存运输更为便捷,也不存在潜在的**形成风险,是较为安全的“细胞外***”方案。目前已有多个针对干细胞外泌体的临床试验在进行,未来有望实现从细胞***向“细胞外***”技术的过渡。外泌体(Exosomes)鉴定+外泌体示踪方法 南京英瀚斯生物。贵州专业的外泌体提取
南京外泌体检测服务,优先南京英瀚斯。山东专门做外泌体检测
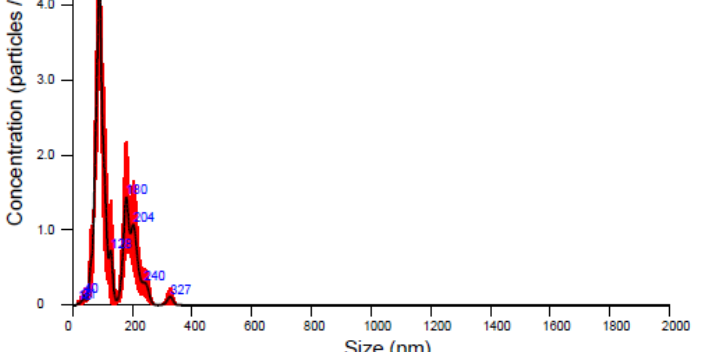
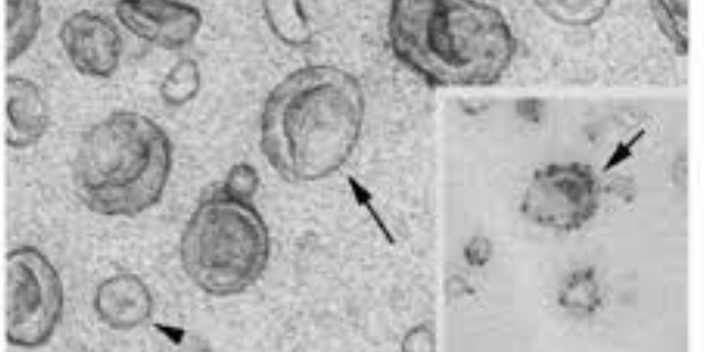
外泌体的分离与鉴定技术是研究和应用的关键步骤,目前常用方法包括超速离心、密度梯度离心、免疫亲和捕获、聚合物沉淀等。其中超速离心法是**经典也是使用**广的方法,能够较好地富集外泌体,但操作复杂、时间长,且容易混杂微囊泡或细胞碎片。近年来,基于商业试剂盒的聚合物沉淀法由于操作便捷、效率较高,也***用于临床样本的初筛研究。而为了提高纯度和特异性,免疫磁珠捕获法结合外泌体特异性表面蛋白(如CD63、CD81等)逐渐成为高通量检测的重要手段。外泌体的鉴定通常需要借助透射电镜(TEM)、纳米颗粒跟踪分析(NTA)和Westernblot等方法综合判断。山东专门做外泌体检测