肝纤维化模型实验动物模型
1.诱导方法:1)成年雄性小鼠40%CCL4,皮下注射或灌胃5mL/kg。每三天/次,连续8周。成年雄性大鼠皮下注射60%CCl4(3ml/kg),每周2次,共9周。2)成年雄性大鼠1%二甲基亚硝胺DMN(10mg/kg),1次/d,2次/周,连续4周。3)成年雄性大鼠腹腔注射硫代乙酰胺(100mg/kg)隔日腹腔注射1次,连续13周。4)成年大鼠,灌胃给白酒7g/kg体重,每日晨1次,连续24周。
英瀚斯生物,一站式动物实验模型服务,专业评估实验结果分析。 英瀚斯生物,实验动物模型多年经验积累!贵州制作实验动物模型是什么
实验动物模型,英瀚斯生物专业做实验外包服务,一站式医学科研平台。目前,抑郁症动物模型,大部分动物模型的建立主要参照以下两个原则之一:对于已知抗抑郁药的作用或者是对应激的反应。目前常用的几种抑郁症动物模型主要分为应激模型、转基因动物抑郁模型、药物诱发的抑郁模型、孤养或分养模型以及其他模型。
抑郁症又称抑郁障碍,以明显而持久的心境低落为主要临床特征,是心境障碍的主要类型。临床可见心境低落与其处境不相称,情绪的消沉可以从闷闷不乐到悲痛欲绝,自卑抑郁,甚至悲观厌世,可有自残企图或行为;部分病例有明显的焦虑和运动性激越;严重者可出现幻觉、妄想等精神bing性症状。每次发作持续至少2周以上、长者甚至数年,多数病例有反复发作的倾向,每次发作大多数可以缓解,部分可有残留症状或转为慢性。 贵州制作实验动物模型是什么英瀚斯生物 实验动物模型整体外包。
实验动物模型,癫痫动物模型。癫痫是一种常见多发的慢性脑部疾病,以脑部神经元过度放电所致的突然出现反复和短暂的中枢的神经系统功能失常为特征。形成癫痫的原因多种多样,病理表现也各不相同。脑电图上的痫性发放和临床发作是癫痫的两个主要特征。痫性发放是局部神经元异常同步化活动在脑电图上的表现。作为大脑神经元活动的一种客观反映,目前通过脑电图检查发现痫样放电,仍是癫痫病诊断和癫痫灶定位的主要客观依据。 由于受条件的限制,人体癫痫脑电数据的样本收集比较困难,而且数据易受外界环境和患者运动的干扰,一些实验在道义和方法上也受到种种制约。如果能够先在实验室建立癫痫动物模型,通过对它进行实验并采集到大量样本,以验证现有算法的正确性,再进一步转向人体数据,就能克服这些不足,缩减科研工作的周期。 鉴于大鼠是医学研究中常用的一种实验动物,并且国内外已有几种可供选择的慢性癫痫模型,因此我们选择成年Wistar大鼠为实验对象,完成慢性颞叶癫痫模型的制备和数据的采集。
阿尔茨海默病实验动物模型。目前常用研究AD的实验动物有非人灵长类动物与啮齿类动物,在选择时遵循“减少、替代、优化”的3R原则。非人灵长类动物与人类的脑部解剖结构、神经病变特点以及生物行为模式相似,尤其是恒河猴,在其脑中观察到含有Aβ沉积的老年斑和神经原纤维缠结现象,无论是自发还是诱发模型,都能够较好的复制AD相关的病理及生理特征,但是昂贵的费用与稀少的资源限制了非人灵长类动物的大量应用。啮齿类动物虽然在病变模拟方面不如非人灵长类全方面的,但是具有价格低廉、资源范围很广的、生存率高等特点,与人类的脑部解剖结构与生理特征也较为相近,更适于诱导模型的大量制备,成为AD应用更范围很广的的动物模型。许多AD小鼠模型的背景品系是C57BL/6J小鼠,然而这种品系的小鼠似乎对类似AD的神经病理学具有特别的抵抗力。有推荐的实验动物模型供应商吗?

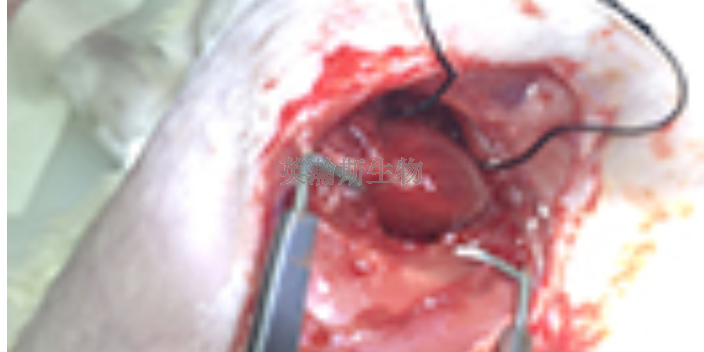
肝切除实验动物模型造模方法:大小鼠的肝叶形状和大小不同。因此,切除每个肺叶需要特别注意其独特的形状和血管位置。左外侧叶很容易切除,因为它有一个狭窄的包含门静脉和肝静脉的蒂,并且不与下腔静脉旁肝相连。然而,如果切除***于切除左侧肝外叶(30%切除模型),则必须在肝左门区分离左侧正中门静脉和伴随的肝动脉。
英瀚斯具备专业动物房、动物实验室、造模操作人员,承接实验动物模型。
由于正中叶在腔静脉周围有一个较宽的半基部,切除该叶需要在距腔静脉3mm的距离处进行几次夹持。单纯结扎肝叶的宽基部切除术有很高的风险导致腔静脉收缩和残端肝组织损伤,因为大量结扎容易导致剩余肝组织变形。由于右上叶位于腔静脉上,基部非常宽,并向背侧延伸至右腔静脉旁肝组织,因此技术上**难切除。切除需要小心地将夹钳放置在离腔静脉3毫米的距离处,并使用4或5条穿刺缝线,以避免损伤残端和腔静脉旁肝组织(图6)。由于约70%的下腔静脉旁组织由右上门静脉的一个分支供应,这种潜在的损伤可能对小的残肝非常重要。 实验动物模型制作周期多久?安徽小鼠实验动物模型制作
英瀚斯实验动物模型,消化系统、呼吸系统、生殖系统各类模型。贵州制作实验动物模型是什么
新一代AD(阿尔兹海默症)实验动物模型。尽管APP-Tg小鼠在过去十几年中范围广的被用于开发新的AD医疗策略,但这种小鼠的基因表型和AD患者的还是不同。而且上述的转基因动物模型在Aβ的生成、tau蛋白的过度磷酸化、神经纤维缠结等病理特征上和AD患者的差异也很大,无法理想地模拟AD患者。为了克服这些不希望出现的问题,研究人员构建了带有Swedish(KM670/671NL)、Beyreuther/Iberian(I716F)和Arctic突变等APP基因敲入(APP-KI)小鼠。APP-KI小鼠在没有过度表达APP的情况下生成Aβ42。随着年龄的增长,APP-KI小鼠大脑皮层和海马区出现过多的Aβ沉积。另一方面,与其他AD模型一样,该模型没有tau病理、NFTs、神经退行性变或大量神经元丢失可用于研究临床前AD。由于基因组编辑的新的进展,尤其是CRISPR/Cas技术,未来对转基因动物模型进行改良也值得期待。贵州制作实验动物模型是什么