●原因:①组织脱水,透明不够。②浸蜡时间过长、浸蜡温度过高。③组织脱出是由于脱水、透明时间不够,或组织中含有乙醇等,石蜡不易渗入组织中故导致石蜡与组织分离。④二甲苯使用时间过久。●解决方法:①必须按组织大小厚薄选择脱水、透明时间。②依组织的性质和结构特点确定浸蜡时间、控制包埋温度。一般这种情况难以补救。③脱水,透明渗蜡不够,应重新熔化,退回入二甲苯和酒精,再进行渗蜡包埋。④更换二甲苯。2.切片皱褶太多且不能完全展开●原因:①石蜡太软或室温过高。②切片刀上粘有残余的石蜡,刀口不干净。③组织浸蜡时间不够或脱水、透明不够。④切片刀不锋利。●解决方法:①可将蜡块放入冰箱中冰冻后切片。并在切片时一边切片一边用冰块冰冻或换蜡。如室温过高,可开空调降低室温。②切片刀不干净,可用棉花沾少许二甲苯将刀口拭干净。③组织浸蜡不够,可重复浸蜡过程。④将切片刀磨锐利再行切片。南京英瀚斯,专业的病理染色实验服务平台。病理实验外包检测,公司自有实验室,欢迎考察。天津真实病理实验外包公司

病理实验外包,病理染色组织处理的要求:恰当的组织处理是做好免疫组化染色的先决条件,也是决定染色成败的内部因素,在组织细胞材料准备的过程中,不仅要求保持组织细胞形态完整,更要保持组织细胞的抗原性不受损或弥漫,防止组织自溶。如果出现自溶坏死的组织,抗原已经丢失,即使用很灵敏的检测抗体和高超的技术,也很难检出所需的抗原,反而往往由于组织的坏死或制片时的刀痕挤压,在上述区域易出现假阳性结果。组织及时取材和固定组织标本及时的取材和固定是做好免疫组化染色的关键第一步,是有效防止组织自溶坏死,抗原丢失的开始,离体组织应尽快的进行取材,比较好2h内,取材时所用的刀应锐利,要一刀下去切开组织,不可反复切拉组织,造成组织的挤压,组织块大小要适中,一般在2.5cm×2.5cm×0.2cm,切记取材时组织块宁可面积大,千万不能厚的原则,(也就是说组织块的面积可以大到3cm×5cm,但组织块的厚度千万不能超过0.2cm,否则将不利于组织的均匀固定)。固定液快速渗透到组织内部使组织蛋白能在一定时间内迅速凝固。从而完好的保存抗原和组织细胞形态。广东真实病理实验外包实验室病理实验外包检测,免疫荧光染色,医学科研实验服务。
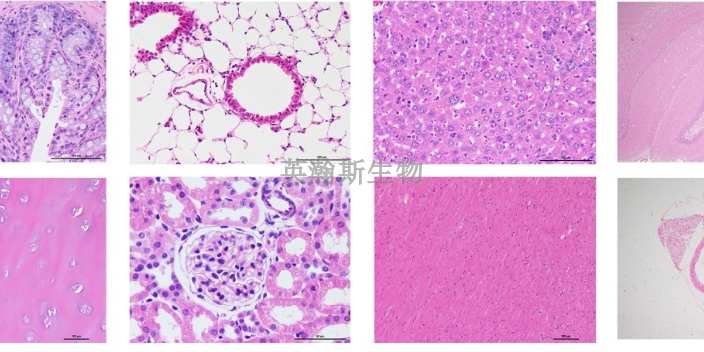
病理实验外包,病理染色多聚甲醛保存组织的注意事项:多聚甲醛放置过久其中的醛基可能会被氧化为酸,使溶液pH降低,从而影响染色。不同细胞或组织样品所需的固定时间有所不同,应当根据细胞或组织的种类以及组织块的大小来调整固定时间。多聚甲醛虽然作用温和,但能硬化组织,固定时间过久会导致组织变脆,切片时易碎。因此固定时间通常不宜超过24小时。多聚甲醛可长期存在于固定过的细胞或组织样品中,固定完成后用适当的洗涤液或水冲洗数小时仍会有残留,因此后续实验结果如果受醛基影响,须尽量洗去残留的多聚甲醛。醛基与抗原蛋白的氨基交联形成羧甲基,使抗原决定簇的三维构象出现空间障碍。分子间交联形成的网格结构可能部分或完全掩盖某些抗原决定簇,使之不能充分暴露,可造成假阴性的染色,影响免疫组化结果。因此,4%多聚甲醛固定的细胞或组织样品在进行免疫组化检测时,有时需要对抗原先进行修复,然后才能进行免疫染色等后续操作。
病理实验外包,病理染色方法分为石蜡切片法和冰冻切片两种,详细的实验方法如下:石蜡切片法实验方法及原理:石蜡切片是比较基本的切片技术,冰冻切片和超薄切片等都是在石蜡切片基础上发展起来的。苏木素与伊红对比染色法(简称H.E.对染法)是组织切片比较常用的染色方法。这种方法适用范围普遍,对组织细胞的各种成分都可着色,便于普遍观察组织构造,而且适用于各种固定液固定的材料,染色后不易褪色可长期保存。冰冻切片试验方法及原理:冰冻切片是指将组织在冷冻状态下直接用切片机切片。它实际上是以水为包埋剂,将组织进行冰冻至坚硬后切片的。在冰冻切片前组织不经过任何化学药品处理或加热过程,明显缩短了制片时间。同时,由于此法不需要经过脱水、透明和浸蜡等步骤,因而较适合于脂肪、神经组织和一些组织化学的制片,并作为快速切片的方法应用在临床诊断。南京英瀚斯,病理实验外包检测,只做真实实验。

病理实验外包,病理染色黏液物质(黏多糖)染色1.Mowry阿尔辛蓝过碘酸雪夫(ABPAS)染色法(1956)红色:中性黏液物质蓝色:酸性黏液物质紫红色:混合性黏液物质2.爱先蓝(PH2.5)法蓝色:唾液酸、弱硫酸化黏液物质、一般粘液红色:胞核不着色:强硫酸化黏液物质3、爱先蓝(PH1.0)法蓝色:含硫酸黏液物质不着色:非硫酸化酸性黏液物质红色:复染后的胞核南京英瀚斯,专业的病理染色实验服务平台。细胞组技术人员毕业于东南大学、华中科技大学等**高校生物学相关专业,具有硕士研究生以上学历,熟练掌握细胞学相关实验,可开展多种细胞实验
病理实验外包,医学实验外包,动物实验外包,就找南京英瀚斯。天津真实病理实验外包公司
病理实验外包,病理染色HE染色常见问题:Q5:细胞核呈棕红色改变答:苏木素染液过度氧化;或苏木素染色后反蓝不足导致。应该立即更换苏木素染色液。或在流动自来水(一般自来水PH7.5-7.8),或在稀释的氨水溶液,或在0.2%碳酸氢钠中适当浸泡,这些步骤均可一定程度地加强苏木素染色后的反蓝效果。Q6:伊红染色较淡答:伊红的PH改变了(PH可能已大于5);或反蓝液体未漂洗干净,残留后影响胞浆嗜酸性染色;或者切片太薄并且在随后的脱水步骤停留过久。对策:检查伊红染色液PH,可采用乙酸调至4.6-5.0。根据以上提示,调整实验步骤。天津真实病理实验外包公司